
Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
Ischémie cérébrale chez le nouveau-né: symptômes, conséquences, traitement
Expert médical de l'article
Dernière revue: 12.07.2025
Une perturbation de la circulation sanguine dans le système vasculaire du cerveau de l'enfant immédiatement après la naissance, provoquant un manque d'oxygène dans le sang (hypoxémie), est définie comme une ischémie cérébrale chez le nouveau-né. Code CIM-10 - P91.0.
Étant donné que l'ischémie, l'hypoxémie et l'hypoxie (manque d'oxygène) sont physiologiquement interconnectées (alors que l'hypoxie peut se développer avec un flux sanguin cérébral normal), l'état critique de carence en oxygène pour le cerveau des nouveau-nés est considéré comme un syndrome clinique en neurologie et est appelé encéphalopathie hypoxique-ischémique néonatale, se développant dans les 12 à 36 heures suivant la naissance.
Épidémiologie
En neurologie néonatale et en pédiatrie, l'épidémiologie des manifestations cliniques de l'ischémie cérébrale chez les nouveau-nés n'est pas enregistrée séparément du syndrome d'encéphalopathie hypoxique-ischémique. Par conséquent, l'évaluation de la morbidité est problématique en raison du manque de critères de différenciation.
L'incidence de l'encéphalopathie néonatale associée à une diminution du débit sanguin cérébral et à une hypoxie cérébrale est estimée à 2,7-3,3 % des cas pour mille enfants nés vivants. Parallèlement, 5 % des enfants atteints de pathologies cérébrales infantiles ont subi un accident vasculaire cérébral périnatal (un cas est diagnostiqué pour 4 500 à 5 000 nourrissons atteints de pathologie hémodynamique cérébrale).
L'incidence de l'asphyxie périnatale est estimée à un à six cas pour mille nouveau-nés à terme et à deux à dix cas chez les prématurés. Les estimations mondiales varient considérablement: selon certaines données, l'asphyxie néonatale est responsable de 840 000 décès, soit 23 % des décès néonatals dans le monde chaque année, tandis que selon les données de l'OMS, elle en cause au moins 4 millions, soit 38 % de tous les décès d'enfants de moins de cinq ans.
Les experts de l'Académie américaine de pédiatrie ont conclu que la meilleure estimation de l'incidence des pathologies cérébrales néonatales repose sur les données démographiques: en moyenne, trois cas pour mille personnes. Selon certains neurophysiologistes occidentaux, certaines conséquences de l'encéphalopathie hypoxique-ischémique contractée à la naissance sont observées chez 30 % de la population des pays développés et plus de la moitié des habitants des pays en développement.
Causes de l'ischémie cérébrale chez le nouveau-né.
Le cerveau a besoin d'un apport constant de sang oxygéné; chez les nourrissons, il représente jusqu'à 10 % du poids corporel, possède un système vasculaire ramifié et consomme un cinquième de l'oxygène fourni par le sang à tous les tissus de l'organisme. Lorsque la perfusion et l'oxygénation cérébrales sont réduites, le tissu cérébral perd la source de survie de ses cellules, et les causes d'ischémie cérébrale chez les nouveau-nés connues à ce jour sont nombreuses. Parmi celles-ci, on peut citer:
- hypoxémie maternelle due à une ventilation insuffisante des poumons dans les maladies cardiovasculaires, l'insuffisance respiratoire chronique ou la pneumonie;
- diminution du flux sanguin vers le cerveau du fœtus et hypoxémie/hypoxie due à des troubles placentaires, notamment thrombose, décollement placentaire et infection;
- clampage prolongé du cordon ombilical pendant l'accouchement, entraînant une acidose métabolique sévère du sang du cordon ombilical, une diminution systémique du volume sanguin circulant (hypovolémie), une chute de la pression artérielle et une altération de la perfusion cérébrale;
- accident vasculaire cérébral aigu (AVC périnatal ou néonatal), qui survient chez le fœtus à partir de la 20e semaine de grossesse et chez le nouveau-né - dans les quatre semaines suivant la naissance;
- absence d’autorégulation automatique du flux sanguin cérébral chez les prématurés;
- violation de la circulation intra-utérine fœtale due à un rétrécissement de l'artère pulmonaire ou à des anomalies cardiaques congénitales (hypoplasie gauche du cœur, persistance du canal artériel, transposition des gros vaisseaux, etc.).
Facteurs de risque
Il existe également de nombreux facteurs de risque de développement d'une ischémie cérébrale chez le nouveau-né, parmi lesquels les neurologues et les obstétriciens notent:
- première grossesse à plus de 35 ans ou à moins de 18 ans;
- thérapie d'infertilité à long terme;
- poids corporel insuffisant du nouveau-né (moins de 1,5 à 1,7 kg);
- accouchement prématuré (avant 37 semaines de grossesse) ou grossesse post-terme (plus de 42 semaines);
- rupture spontanée des membranes;
- travail trop long ou trop rapide;
- présentation anormale du fœtus;
- vasa praevia, le plus souvent observé lors de la fécondation in vitro;
- traumatisme du crâne du nourrisson lors de l’accouchement (suite à des erreurs obstétricales);
- césarienne d'urgence;
- saignements abondants pendant l'accouchement;
- la présence de maladies cardiovasculaires ou auto-immunes, d'anémie, de diabète sucré, de troubles fonctionnels de la glande thyroïde, de troubles de la coagulation sanguine (thrombophilie), de syndrome des antiphospholipides, de maladies infectieuses et inflammatoires des organes pelviens chez la femme enceinte;
- hypotension artérielle sévère pendant la grossesse et gestose tardive.
Les pathologies sanguines congénitales associées à des mutations dans les gènes de la prothrombine, des facteurs de coagulation plaquettaire V et VIII, de l'homocystéine plasmatique, ainsi que le syndrome DIC et la polyglobulie sont également reconnus comme des facteurs de risque d'ischémie cérébrale chez les nourrissons.
Pathogénèse
L'ischémie cérébrale du nouveau-né perturbe le métabolisme des cellules cérébrales, ce qui entraîne une destruction irréversible de la structure du tissu nerveux et son dysfonctionnement. Tout d'abord, la pathogenèse du développement de ces processus destructeurs est associée à une chute rapide du taux d'adénosine triphosphate (ATP), principal fournisseur d'énergie pour tous les processus biochimiques.
L'équilibre entre les concentrations intracellulaires et extracellulaires des ions traversant leurs membranes est également important pour le fonctionnement normal des neurones. Lorsque le cerveau est privé d'oxygène, le gradient transmembranaire d'ions potassium (K+) et sodium (Na+) dans les neurones est perturbé, et la concentration extracellulaire de K+ augmente, entraînant une dépolarisation anoxydative progressive. Parallèlement, l'afflux d'ions calcium (Ca2+) augmente, initiant la libération du neurotransmetteur glutamate, qui agit sur les récepteurs NMDA du cerveau; leur stimulation excessive (excitotoxicité) entraîne des modifications morphologiques et structurelles du cerveau.
L'activité des enzymes hydrolytiques, qui dégradent les acides nucléiques des cellules et provoquent leur autolyse, augmente également. Dans ce cas, la base des acides nucléiques, l'hypoxanthine, se transforme en acide urique, accélérant la formation de radicaux libres (formes actives de l'oxygène et de l'oxyde d'azote) et d'autres composés toxiques pour le cerveau. Les mécanismes de protection antioxydante du cerveau des nouveau-nés ne sont pas encore totalement développés, et la combinaison de ces processus a un effet extrêmement négatif sur ses cellules: gliose neuronale, atrophie des cellules gliales et des oligodendrocytes de la substance blanche.
Symptômes de l'ischémie cérébrale chez le nouveau-né.
Les symptômes cliniques de l'ischémie cérébrale chez les nouveau-nés et l'intensité de leur manifestation sont déterminés par son type, sa gravité et la localisation des zones de nécrose neuronale.
Les types d’ischémie comprennent des lésions focales ou topographiquement limitées du tissu cérébral, ainsi que des lésions globales qui s’étendent à de nombreuses structures cérébrovasculaires.
Les premiers signes d'ischémie cérébrale à la naissance peuvent être détectés par l'examen des réflexes d'automatisme spinal congénital. Cependant, l'évaluation de leurs anomalies dépend du degré de trouble de la perfusion cérébrale et de la maturité physiologique du nouveau-né.
Étapes
Ainsi, l'ischémie cérébrale du premier degré chez le nouveau-né (forme légère d'encéphalopathie hypoxique-ischémique) se manifeste chez le nourrisson né à terme par une augmentation modérée du tonus musculaire et des réflexes tendineux (réflexes de préhension, de Moro, etc.). Les symptômes comprennent également une anxiété excessive avec mouvements fréquents des membres, des myoclonies post-hypoxiques (contractions musculaires isolées sur fond de rigidité musculaire), des troubles de l'attachement au sein, des pleurs spontanés et un sommeil intermittent.
Si l'enfant est né prématurément, outre une diminution des réflexes inconditionnés (moteurs et de succion), on observe un affaiblissement du tonus musculaire général au cours des premiers jours suivant la naissance. En règle générale, il s'agit d'anomalies temporaires; si l'état du système nerveux central du nourrisson se stabilise en quelques jours, l'ischémie n'entraîne pratiquement pas de complications neurologiques. Cependant, tout dépend de l'activité régénératrice endogène du cerveau en développement de l'enfant, ainsi que de la production de neurotrophines cérébrales et de facteurs de croissance épidermiques et insulino-analogues.
L'ischémie cérébrale du 2e degré chez le nouveau-né (provoquant une forme modérément sévère d'encéphalopathie hypoxique-ischémique) s'ajoute à la liste des symptômes déjà mentionnés: crises d'épilepsie; diminution de la pression artérielle et augmentation de la pression cérébrale (on observe une dilatation et une pulsation notable de la fontanelle); léthargie pendant l'alimentation et régurgitations fréquentes; troubles intestinaux; périodes de troubles du rythme cardiaque et d'apnée (arrêt respiratoire pendant le sommeil); cyanose labile et effet « peau marbrée » (dus à des troubles végétatifs-vasculaires). La période aiguë dure environ dix jours. De plus, les néonatologistes notent la possibilité de complications telles qu'une hydrocéphalie, des troubles du mouvement oculaire ( nystagmus ) et un strabisme.
En cas d'ischémie cérébrale de grade 3 chez un nouveau-né, les réflexes néonatals (succion, déglutition, préhension) sont absents et les crises sont fréquentes et prolongées (dans les 24 à 48 heures suivant la naissance). Elles diminuent ensuite, laissant place à une diminution progressive du tonus musculaire, à un état de stupeur et à une augmentation de l'œdème cérébral.
Selon la localisation des principaux foyers d'ischémie cérébrale, on peut observer un dysfonctionnement respiratoire (le nourrisson nécessite souvent une assistance respiratoire mécanique), des modifications du rythme cardiaque, des pupilles dilatées (peu sensibles à la lumière) et un manque de conjugaison oculomotrice (« yeux de poupée »).
Ces manifestations sont en augmentation, indiquant le développement d'une encéphalopathie hypoxique-ischémique sévère, qui, en raison d'une insuffisance cardiorespiratoire, peut être mortelle.
 [ 30 ]
[ 30 ]
Complications et conséquences
Le développement d'une ischémie cérébrale chez le nouveau-né provoque des lésions de ses cellules par manque d'oxygène et conduit à des conséquences et complications neurologiques très graves, souvent irréversibles, qui sont corrélées à la topographie des lésions.
Comme l'ont montré des études, les cellules pyramidales de l'hippocampe, les cellules de Purkinje du cervelet, les neurones réticulaires de la région péri-rolandique du cortex cérébral et de la partie ventrolatérale du thalamus, les cellules des noyaux gris centraux, les fibres nerveuses du tractus corticospinal, les noyaux du mésencéphale, ainsi que les neurones du néocortex et du tronc cérébral sont plus sensibles à l'ischémie cérébrale chez les nouveau-nés.
Chez les nouveau-nés à terme, le cortex cérébral et les noyaux profonds sont principalement touchés; chez les prématurés, on observe une destruction diffuse des cellules de la substance blanche dans les hémisphères, ce qui provoque une invalidité chronique chez les enfants survivants.
Et avec l'ischémie globale des cellules du tronc cérébral (où sont concentrés les centres de régulation de la respiration et de la fonction cardiaque), leur mort totale et leur mort presque inévitable se produisent.
Les conséquences négatives et les complications de l'ischémie cérébrale périnatale et néonatale de degré 2-3 chez le jeune enfant se manifestent par une épilepsie, une perte unilatérale de la vision, un retard du développement psychomoteur, des troubles moteurs et cognitifs, dont une paralysie cérébrale. Dans de nombreux cas, leur gravité peut être pleinement évaluée dès l'âge de trois ans.
 [ 31 ]
[ 31 ]
Diagnostics de l'ischémie cérébrale chez le nouveau-né.
Le diagnostic initial d'ischémie cérébrale chez le nouveau-né est réalisé immédiatement après la naissance, lors d'un examen standard de l'enfant et de la détermination de son état neurologique (selon l'échelle d'Apgar), en vérifiant le degré d'excitabilité réflexe et la présence de certains réflexes congénitaux (dont certains ont été mentionnés lors de la description des symptômes de cette pathologie). La fréquence cardiaque et la tension artérielle sont obligatoirement enregistrées.
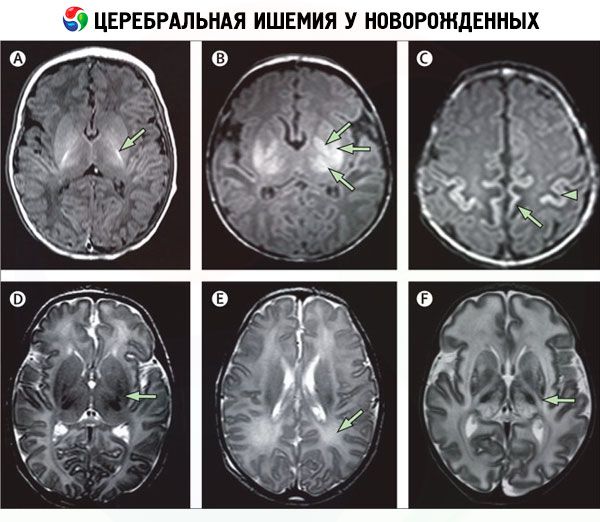
Le diagnostic instrumental, notamment la neurovisualisation, permet d'identifier les zones d'ischémie cérébrale. À cette fin, les techniques suivantes sont utilisées:
- tomodensitométrie des vaisseaux cérébraux (angiographie CT);
- imagerie par résonance magnétique (IRM) du cerveau;
- examen échographique cranio-cérébral (échographie);
- électroencéphalographie (EEG);
- échocardiographie (ECG).
Les examens de laboratoire comprennent une numération formule sanguine complète, ainsi que des analyses sanguines pour déterminer les taux d'électrolytes, le temps de prothrombine et de fibrinogène, l'hématocrite, les gaz du sang artériel et un pH sanguin veineux ou ombilical (pour détecter une acidose). La composition chimique et l'osmolalité des urines sont également analysées.
Diagnostic différentiel
Pour exclure la présence d'une méningo-encéphalite périnatale, d'une tumeur cérébrale, d'une tyrosinémie, d'une homocystinurie, d'un syndrome congénital de Zellweger, d'un trouble du métabolisme du pyruvate, ainsi que de neuropathies mitochondriales génétiquement déterminées, d'acidémie méthylmalonique ou propionique chez le nourrisson, des diagnostics différentiels sont effectués.
Qui contacter?
Traitement de l'ischémie cérébrale chez le nouveau-né.
Dans de nombreux cas, aux premiers stades, le traitement de l'ischémie cérébrale chez les nouveau-nés nécessite une réanimation cardio-pulmonaire chez les nouveau-nés avec ventilation artificielle des poumons et toutes les mesures pour restaurer l'hémodynamique du système vasculaire du cerveau, maintenir l'hémostase et prévenir l'hyperthermie, l'hypo et l'hyperglycémie.
L'hypothermie contrôlée réduit significativement l'ampleur des lésions ischémiques modérées et sévères des cellules cérébrales chez les nourrissons: le corps est refroidi à +33-33,5 °C pendant 72 heures, puis la température corporelle remonte progressivement jusqu'à la normale physiologique. Ce traitement n'est pas utilisé chez les prématurés nés avant 35 semaines.
Le traitement médicamenteux est symptomatique, par exemple, pour les crises tonico-cloniques, les médicaments anticonvulsivants les plus couramment utilisés sont la diphénine (phénytoïne), la triméthine (triméthadione) - deux fois par jour, 0,05 g (avec surveillance systématique de la composition sanguine).
Pour réduire l'hypertonie musculaire après trois mois, le relaxant musculaire tolpérisone (Mydocalm) peut être administré par voie intramusculaire, à raison de 5 à 10 mg par kilogramme de poids corporel (jusqu'à trois fois par jour). Ce médicament peut provoquer des effets secondaires tels que nausées et vomissements, éruptions cutanées et démangeaisons, faiblesse musculaire, suffocation et choc anaphylactique.
L'amélioration de la perfusion cérébrale est facilitée par l'administration intraveineuse de Vinpocetine (la posologie est calculée en fonction du poids corporel).
Pour activer les fonctions cérébrales, il est courant d'utiliser des médicaments neuroprotecteurs et des nootropes: Piracetam (Nootropil, Noocephal, Pyrroxil, Dinacel) – 30 à 50 mg par jour. Le sirop Ceraxon est prescrit à raison de 0,5 ml deux fois par jour. Il convient de noter que ce médicament est contre-indiqué en cas d'hypertonie musculaire et que ses effets secondaires incluent l'urticaire allergique, une baisse de la tension artérielle et des troubles du rythme cardiaque.
En cas de dysfonctionnement du système nerveux central, on utilise du glutan (acide glutamique, aciduline) à raison de 0,1 g trois fois par jour (avec surveillance de la composition sanguine). Les médicaments nootropes à base d'acide hopanténique (sirop de Pantogam) améliorent l'oxygénation du tissu cérébral et présentent des propriétés neuroprotectrices.
Les vitamines B6 (chlorhydrate de pyridoxine) et B12 (cyanocobalamine) sont utilisées par voie parentérale avec une solution de glucose.
Traitement de physiothérapie
En cas d'ischémie cérébrale légère chez un nouveau-né, un traitement de kinésithérapie est indispensable, notamment le massage thérapeutique, qui contribue à réduire l'hypertonie musculaire. Cependant, en cas de syndrome épileptique, le massage n'est pas utilisé.
Améliorez l'état des nouveau-nés atteints d'ischémie cérébrale grâce à des bains à base de décoction de fleurs de camomille, de menthe poivrée ou de menthe citronnée. Traitement à base de plantes – voir Sédatifs pour enfants.
La prévention
Les neurologues estiment que la prévention du syndrome d'encéphalopathie hypoxique-ischémique néonatale est problématique. Il ne s'agit ici que d'un suivi obstétrical approprié pendant la grossesse et d'une détection précoce des facteurs de risque: pathologies cardiovasculaires chez la femme enceinte, troubles endocriniens, troubles de la coagulation sanguine, etc. Un traitement précoce permet de prévenir les effets de l'anémie, de l'hypertension ou de l'hypotension artérielle, ou des maladies infectieuses et inflammatoires. Cependant, de nombreux problèmes ne peuvent être résolus aujourd'hui par les moyens disponibles.
Prévoir
Malheureusement, un pronostic favorable concernant les conséquences de l'ischémie cérébrale chez les nouveau-nés n'est observé que dans sa forme légère.
Les encéphalopathies néonatales sont une cause de mortalité élevée et de pathologies neurologiques à long terme chez les nourrissons dans le monde entier.

